Lưu huỳnh | Khái niệm hoá học
Trong bảng hệ thống tuần hoàn các nguyên tố hóa học, nguyên tố lưu huỳnh nằm ở ô thứ 16, chu kì 3, nhóm VIA và có kí hiệu hóa học là S. Lưu huỳnh là một phi kim phổ biến, dạng tinh khiết có màu vàng chanh. Trong thiên nhiên, nó có thể tìm thấy ở dạng tự do và tập trung ở các vùng có núi lửa như Xixili và Nhật Bản. Nga và Mĩ là những nước có nhiều mỏ lưu huỳnh tự nhiên lớn nhất hiện nay. Trong thương mại, nó được sử dụng rất rộng rãi như làm phân bón, thuốc súng, thuốc trừ sâu và thuốc diệt nấm.
Giới thiệu
1. Tính chất vật lí
Lưu huỳnh tồn tại dưới một số dạng thù hình khác nhau. Hai dạng tinh thể thông thường nhất của lưu huỳnh là dạng tà phương và dạng đơn tà.
Lưu huỳnh tà phương, còn gọi là S có màu vàng, nóng chảy ở 112,8oC và có tỉ khối là 2,06. Nó bền ở nhiệt độ thường, trên 95,5oC chuyển sang dạng đơn tà. Lưu huỳnh tồn tại tự do trong thiên nhiên là lưu huỳnh tà phương.
Lưu huỳnh đơn tà, còn gọi là S, có màu vàng nhạt, nóng chảy ở 119,2oC và có tỉ khối là 1,96. Nó bền trên 95,5oC, dưới nhiệt độ đó chuyển dần sang dạng tà phương.
Lưu huỳnh tà phương và lưu huỳnh đơn tà đều không tan trong nước, rất ít tan trong rượu và ete, tan nhiều trogn dầu hỏa, benzen và nhất là trong cacbon disunfua. Trong các dung môi đó, lưu huỳnh tà phương tan hơi nhiều hơn lưu huỳnh đơn tà. Khi kết tinh từ những dung dịch đó, lưu huỳnh xuất hiện dưới dạng tinh thể tà phương.
Phép xác định khối lượng phân tử của lưu huỳnh trong các dung môi khác nhau bằng phương pháp nghiệm lạnh cho thấy rằng lưu huỳnh tà phương và đơn tà đều gồm những phân tử có tám nguyên tử S8. Tuy nhiên vì lí do động học, trong những phản ứng hóa học có lưu huỳnh tham gia, người ta thường dùng kí hiệu S để chỉ lưu huỳnh chứ không dùng S8.

Phân tử lưu huỳnh, S8
Khi đun đến nóng chảy, lưu huỳnh biến thành một chất lỏng trong suốt linh động và có màu vàng. Đến trên 160oC lưu huỳnh nhanh chóng có màu nâu đỏ và nhớt dần, đến 200oC lưu huỳnh lỏng đặc quánh lại giống như nhựa và có màu nâu đen.

Một mẩu lưu huỳnh nóng chảy thành chất lỏng màu đỏ máu.
2. Tính chất hóa học
Lưu huỳnh là nguyên tố tương đối hoạt động: ở nhiệt độ thường hơi kém hoạt động, nhưng khi đun nóng tương tác với hầu hết các nguyên tố trừ các khí hiếm, nit ơ, iot, vàng và platin.
Đơn chất lưu huỳnh (số oxi hóa 0) là số oxi hóa trung gian giữa -2 với +4 hoặc +6. Vì vậy, lưu huỳnh vừa thể hiện tính khử vừa thể hiện tính oxi hóa. Tuy nhiên, tính oxi hóa vẫn trội hơn tính khử.
a. Tác dụng với Hidro
khi đun nóng ở nhiệt độ 300oC lưu huỳnh tương tác với hidro tạo thành hidro sunfua
S (tà phương) + H2 H2S
b. Tác dụng với kim loại
Lưu huỳnh tác dụng với kim loại tạo thành sunfua kim loại: với các kim loại kiềm, kiềm thổ, bạc, thủy ngân, phản ứng xảy ra ở nhiệt độ thấp, còn với niken, coban,… ở nhiệt độ cao
Hg + S HgS
Ứng dụng dùng để thu hồi thủy ngân.
Như vậy, khi tác dụng với hidro và kim loại, số oxi hóa của nguyên tố S giảm từ 0 xuống -2. Lưu huỳnh thể hiện oxi hóa.
c. Tác dụng với phi kim
Ở nhiệt độ thích hợp, lưu huỳnh tác dụng với một số phi kim như Clo, flo, oxi…
S + O2 SO2
S + F2 SF6
Như vậy, khi tác dụng với các phi kim hoạt động như clo, flo, oxi số oxi hóa của S tăng từ 0 đến +4 hoặc +6. Lưu huỳnh thể hiện tính khử.
3. Ứng dụng
Lưu huỳnh là nguyên liệu quan trọng cho nhiều ngành công nghiệp:
– 90% lượng lưu huỳnh sản xuất được dùng để điều chế H2SO4
– 10% lượng lưu huỳnh còn lại được dùng để lưu hóa cao su, chế tạo diêm, sản xuất chất tẩy trắng bột giấy, chấy dẻo ebonit, dược phẩm, phẩm nhuộm, chất trừ sâu và chất diệt nấm trong công nghiệp…
4. Trạng thái tự nhiên và phương pháp điều chế
Lưu huỳnh là nguyên tố không kim loại duy nhất đã được biết từ thời thượng cổ. Nó thuộc nguyên tố rất phổ biến, chiếm khoảng 0,03% tổng số nguyên tử của vỏ Trái Đất. Trong thiên nhiên nó có thể tồn tại ở trạng thái tự do và tập trung chủ yếu ở các vùng có núi lửa như Xixili và Nhật Bản. Nga và Mĩ là những nước có mỏ lớn lưu huỳnh tự do. Phần lớn, lưu huỳnh tồn tại trong thiên nhiên dưới dạng hợp chất, phổ biến nhất là các khoáng vật sunfua như pirit (FeS2), cancopirit (FeCuS2), galen (PbS), blendo (ZnS) và một số khoáng vật sunfat như thạch cao, baritin, selestin. Trong khí núi lửa và trong nước của một số suối khoáng có chứa hợp chất của lưu huỳnh. Lưu huỳnh còn có trong thành phần của protein cho nên luôn luôn có trong thực vật và động vật.
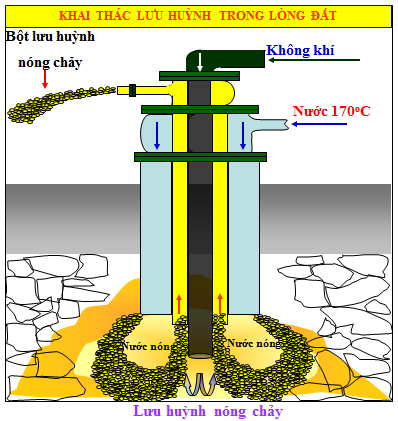
Người ta khai thác lưu huỳnh chủ yếu từ mỏ lưu huỳnh tự do. Nguyên tắc của phương pháp khai thác này là hóa lỏng lưu huỳnh ở ngầm dưới đất rồi bơm lưu huỳnh lỏng lên trên mặt đất.
Ngoài phương pháp trên, lưu huỳnh có thể điều chế bằng cách nhiệt phân pirit FeS2 ở nhiệt độ trên 600oC trong lò hầm
FeS2 FeS + S
Tổng số đánh giá:
Xếp hạng: / 5 sao
Chia sẻ
Các khái niệm hoá học liên quan
Enzim
Enzim là chất xúc tác sinh học được tổng hợp trong các tế bào sống. Enzm chỉ làm tăng tốc độ của phản ứng mà không bị biến đổi sau phản ứng.
Tỉ khối hơi của chất A so với chất B
Tỉ khối là so sánh khối lượng, nghĩa là muốn biết chất nào nặng hơn, chất nào nhẹ hơn và nặng hay nhẹ hơn bao nhiêu lần. Tỉ khối hơi của chất A so với chất B nghĩa là muốn biết ở dạng hơi (hay khí) thì hơi A nặng hay nhẹ hơn hơi (khí) B bao nhiêu lần.
Amin
Amin là dẫn xuất của amoniac, trong đó nguyên tử hidro được thay thế bằng gốc hidrocacbon (no, không no, thơm). Tùy theo số gốc hidrocacbon liên kết với nguyên tử nito mà có các loại amin bậc 1, bậc 2, bậc 3, muối amoni bậc 4. Do phân tử amin có nguyên tử nito còn đôi electron chưa liên kết (tương tự phân tử amoniac) nên amin thể hiện tính bazơ, ngoài ra nitơ trong phân tử amin có số oxi hóa -3 nên amin thường dễ bị oxi hóa. Amin thơm điển hình nhất là anilin có nhiều ứng dụng quan trong trong công nghiệp phẩm nhuộm, polime, dược phẩm..
Xeton
Xeton là những hợp chất hữu cơ mà phân tử có nhóm C=O liên kết trực tiếp với hai nguyên tử cacbon. Nhóm C=O liên kết với 2 nguyên tử cacbon khác là nhóm chức xeton.
Xeton đơn giản và thông dụng nhất là axeton. Axeton được dùng làm dung môi trong quá trình sản xuất nhiều hợp chất trong công nghiệp mĩ phẩm, làm nguyên liệu tổng hợp clorofom, iodofom…
Liên kết hiđro
Liên kết hidro là một loại liên kết yếu được hình thành khi nguyên tử hidro đã tham gia liên kết cộng hóa trị với nguyên tử của một nguyên tố âm điện mạnh lại tương tác với một nguyên tử âm điện khác có cặp electron chưa liên kết (chưa chia).
Một số định nghĩa cơ bản trong hoá học.
Mol là gì?
Trong hóa học, khái niệm mol được dùng để đo lượng chất có chứa 6,022.10²³ số hạt đơn vị nguyên tử hoặc phân tử chất đó. Số 6,02214129×10²³ – được gọi là hằng số Avogadro.
Độ âm điện là gì?
Độ âm điện là đại lượng đặc trưng định lượng cho khả năng của một nguyên tử trong phân tử hút electron (liên kết) về phía mình.
Kim loại là gì?
Kim loại (tiếng Hy Lạp là metallon) là nguyên tố có thể tạo ra các ion dương (cation) và có các liên kết kim loại, và đôi khi người ta cho rằng nó tương tự như là cation trong đám mây các điện tử.
Nguyên tử là gì?
Nguyên tử là hạt nhỏ nhất của nguyên tố hóa học không thể chia nhỏ hơn được nữa về mặt hóa học.
Phi kim là gì?
Phi kim là những nguyên tố hóa học dễ nhận electron; ngoại trừ hiđrô, phi kim nằm bên phải bảng tuần hoàn.
Những sự thật thú vị về hoá học có thể bạn chưa biết
Sự thật thú vị về Hidro
Hydro là nguyên tố đầu tiên trong bảng tuần hoàn. Nó là nguyên tử đơn giản nhất có thể bao gồm một proton trong hạt nhân được quay quanh bởi một electron duy nhất. Hydro là nguyên tố nhẹ nhất trong số các nguyên tố và là nguyên tố phong phú nhất trong vũ trụ.
Sự thật thú vị về heli
Heli là một mặt hàng công nghiệp có nhiều công dụng quan trọng hơn bong bóng tiệc tùng và khiến giọng nói của bạn trở nên vui nhộn. Việc sử dụng nó là rất cần thiết trong y học, khí đốt cho máy bay, tên lửa điều áp và các tàu vũ trụ khác, nghiên cứu đông lạnh, laser, túi khí xe cộ, và làm chất làm mát cho lò phản ứng hạt nhân và nam châm siêu dẫn trong máy quét MRI. Các đặc tính của heli khiến nó trở nên không thể thiếu và trong nhiều trường hợp không có chất nào thay thế được heli.
Sự thật thú vị về Lithium
Lithium là kim loại kiềm rất hoạt động về mặt hóa học, là kim loại mềm nhất. Lithium là một trong ba nguyên tố được tạo ra trong BigBang! Dưới đây là 20 sự thật thú vị về nguyên tố Lithium – một kim loại tuyệt vời!
Sự thật thú vị về Berili
Berili (Be) có số nguyên tử là 4 và 4 proton trong hạt nhân của nó, nhưng nó cực kỳ hiếm cả trên Trái đất và trong vũ trụ. Kim loại kiềm thổ này chỉ xảy ra tự nhiên với các nguyên tố khác trong các hợp chất.
Sự thật thú vị về Boron
Boron là nguyên tố thứ năm của bảng tuần hoàn, là một nguyên tố bán kim loại màu đen. Các hợp chất của nó đã được sử dụng hàng nghìn năm, nhưng bản thân nguyên tố này vẫn chưa bị cô lập cho đến đầu thế kỉ XIX.
So sánh các chất hoá học phổ biến.
FeSi và CaO2. 8H2O
Điểm khác nhau về tính chất vật lý, hoá học giữa chất Sắt silicua và chất Canxi peroxit octahidrat
B2S3 và NaAlCl4
Điểm khác nhau về tính chất vật lý, hoá học giữa chất Dibo trisunfua và chất Natri tetracloroaluminat
K2S2O7 và Pd
Điểm khác nhau về tính chất vật lý, hoá học giữa chất Đikali đisunfat và chất Paladi
K2SiF6 và K3AlF6
Điểm khác nhau về tính chất vật lý, hoá học giữa chất Kali hexaflorosilicat và chất Kali Hexafloroaluminat