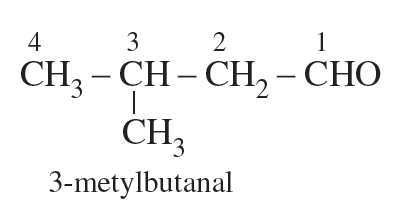Aldehyde | Khái niệm hoá học
Aldehyde là những hợp chất hữu cơ mà phân tử có nhóm -CH=O liên kết trực tiếp với nguyên tử cacbon hoặc nguyên tử hidro. Aldehyde đơn giản nhất là fomaldehyde. Nhiều aldehyde có nguồn gốc thiên nhiên được dùng làm hương liệu trong công nghiệp thực phẩm, mĩ phẩm như geranial (trong tinh dầu hoa hồng), xitrolenal (trong tinh dầu bạch đàn), vanilin, piperonal….
Giới thiệu
1. Định nghĩa
Aldehyde là những hợp chất hữu cơ mà phân tử có nhóm -CH=O liên kết trực tiếp với nguyên tử cacbon hoặc nguyên tử hidro.
Thí dụ, H-CH=O: Aldehyde fomic (metanal); CH3-CH=O: Aldehyde axetic (Etanal)..
Nhóm -CH=O là nhóm chức aldehyde.
2. Phân loại
Dựa theo đặc điểm cấu tạo của gốc hydrocacbon và theo số nhóm -CHO trong phân tử, người ta chia thành aldehyde no, không no, thơm; aldehyde đơn chức, đa chức.
Thí dụ:
Aldehyde no, mạch hở, đơn chức là hợp chất trong phân tử có một nhóm -CH=O liên kết với gốc alkyl hoặc nguyên tử hydro. Các chất H-CH=O; CH3-CHO; CH3CH2-CHO,… lập thành dãy đồng đẳng aldehyde no, mạch hở, đơn chức, có công thức cấu tạo thu gon là CxH2x+1-CHO (x≥0) hay công thức chung CnH2nO (n≥1)
3. Danh pháp
– Tên thay thế của các aldehyde no, đơn chức, mạch hở được cấu tạo như sau:
Tên hydrocarbon no tương ứng với mạch chính + al
Mạch chính của phân tử aldehyde là mạch carbon dài nhất bắt đầu từ nhóm -CHO
– Một số aldehyde có tên thông thường: aldehyde + tên acid tương ứng
Tên một số aldehyde no, đơn chức được trình bày dưới đây
4. Đặc điểm cấu tạo
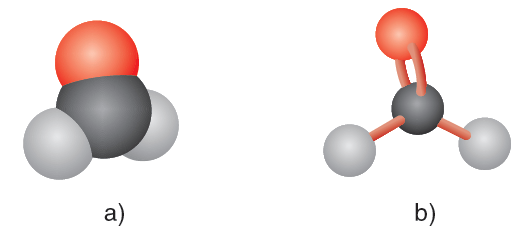
Nhóm -CHO có cấu tạo như sau:
Trong nhóm -CHO, liên kết đôi C=O gồm một liên kết σ bền và một liên kết π kém bền hơn, tương tự liên kết đôi C=C trong phân tử alken, do đó aldehdye có một số tính chất giống alken.
5. Tính chất vật lý
Ở điều kiện thường, các aldehyde đầu dãy đồng đẵng là chất khí (HCHO sôi ở -19oC, CH3CHO sôi ở 21oC) và tan rất tốt trong nước. Các aldehyde tiếp theo là chất lỏng hoặc chất rắn, độ tan trong nước của chúng giảm dần theo chiều tăng của phân tử khối.
Dung dịch nước của aldehyde fomic được gọi là fomon. Dung dịch bão hòa của aldehyde fomic (Có nồng độ 37-40%) được gọi là fomalin.
6. Tính chất hóa học
a. Phản ứng với các amin
Aldehyd +amin → Imine+ nước
b. Phản ứng với alcol
CH3-CHO+CH3-CH2-OH → CH3-CH(OH)-CH2-CHO
d. Phản ứng cộng hạt nhân
e. Phản ứng khử (Phản ứng cộng với hidro)
Aldehyd cộng hidro (xúc tác Niken) đun nóng tạo ra ancol bậc I.
R-CHO + H2 → R-CH2OH
f. Phản ứng oxi hóa
– Phản ứng đặc trưng của aldehyd là phản ứng tráng gương:
R-CHO + 2[Ag(NH3)2]OH → R-COONH4 + 2Ag + 3NH3 + H2O.
Riêng HCHO có thể phản ứng tráng gương với tỉ lệ 1:4
HCHO + 4[Ag(NH3)2]OH → (NH4)2CO3 + 4Ag + 6NH3 + 2H2O.
– Các aldehyd còn tác dụng được với Cu(OH)2 trong môi trường kiềm cho kết tủa Cu2O màu đỏ gạch:
R-CH=O + 2Cu(OH)2 + NaOH → R-COONa + Cu2O + 3H2O
Riêng đối với HCHO:
HCHO + 4Cu(OH)2 + 2NaOH → Na2CO3 + 2Cu2O + 6H2O
Các aldehyd đa chức phản ứng theo tỉ lệ 1:2n (n là số chức -CHO).
– Ngoài ra aldehyd còn có phản ứng với dung dịch brom:
R-CHO + Br2 + H2O → R-COOH + 2HBr.
– Aldehyd cũng có thể làm mất màu dung dịch thuốc tím KMnO4.
R-CHO + KMnO4 → RCOOK + MnO2 + H2O.
Aldehyd có phản ứng oxi hóa bởi O2 tạo ra axit cacboxylic tương ứng với xúc tác Mn2+ và ở nhiệt độ cao:
.
Các phản ứng: tráng gương, làm mất màu dung dịch brom, làm mất màu dung dịch thuốc tím dùng để nhận biết aldehye
7. Ứng dụng
Fomaldehyde được dùng làm nguyên liệu sản xuất nhựa phenol-fomaldehyde, nhựa ure-fomaldehyde.
Dung dịch nước cảu fomaldehyde (fomon) được dùng làm chất tẩy uế, ngâm mẫu động vật làm tiêu bản, dùng trong kĩ nghệ da giày do có tính sát trùng.
Aldehyde acetic được dùng để sản xuất acid acetic làm nguyên liệu cho nhiều ngành sản xuất.
Nhiều aldehyde có nguồn gốc thiên nhiên được dùng làm hương liệu trong công nghiệp thực phẩm, mĩ phẩm như geranial (Trong tinh dầu hoa hồng)….
Tổng số đánh giá:
Xếp hạng: / 5 sao
Chia sẻ
Các khái niệm hoá học liên quan
Glucose
Glucose (còn gọi là dextrose ) là một loại monosaccarit với công thức phân tử C6H12O6 và phổ biến nhất. Trong tự nhiên, glucose có nhiều trong quả nho chính nên còn gọi là đường nho. Glucose là chất dinh dưỡng có giá trị của con người, nhất là đối với trẻ em, người già. Trong y học, glucose được dùng làm thuốc tăng lực.
Natri azua
Sodium Azide (natri azua, muối azua) dạng bột trắng, tơi xốp, tan trong nước, được ứng dụng sản xuất trong công nghiệp như chất tạo khí trong túi hơi an toàn trong xe ô tô, phụ gia trong sản các chế phẩm hóa học, pháo hoa, quốc phòng, chất diệt khuẩn, nấm mốc.
Một số protein đơn giản và quan trọng
Chất đạm Protein là chất dinh dưỡng thiết yếu của cơ thể con người cũng như cơ thể các động vật nói chung. Chất đạm cung cấp các thành tố để cấu trúc nên cơ thể sinh học cũng như là nguồn năng lượng rất quan trọng cho các hoạt động sự sống. Protein được cấu tạo các acid amin.Protein đơn giản có vai trò hết sức quan trọng đối với cơ thể con người.
Hợp chất đa chức
Hợp chất đa chức là hợp chất hữu cơ trong phân tử chứa từ 2 nhóm chức giống nhau trở lên.
Chuẩn độ ngược là gì?
Trong phương pháp chuẩn độ, có 3 kỹ thuật chuẩn độ hay dùng đó là chuẩn độ trực tiếp, chuẩn độ thay thế và chuẩn độ ngược.
Chuẩn độ ngược (còn được gọi là chuẩn độ thừa trừ) là kỹ thuật chuẩn độ thêm một thể tích chính xác và dư dung dịch chuẩn độ vào dung dịch chất cần định lượng. Sau đó xác định lượng dư của thuốc thử bằng một thuốc thử khác thích hợp. Dựa vào thể tích và nồng độ của hai thuốc thử đã dùng cùng với phản ứng chuẩn độ để tính lượng chất cần định lượng.
Một số định nghĩa cơ bản trong hoá học.
Mol là gì?
Trong hóa học, khái niệm mol được dùng để đo lượng chất có chứa 6,022.10²³ số hạt đơn vị nguyên tử hoặc phân tử chất đó. Số 6,02214129×10²³ – được gọi là hằng số Avogadro.
Độ âm điện là gì?
Độ âm điện là đại lượng đặc trưng định lượng cho khả năng của một nguyên tử trong phân tử hút electron (liên kết) về phía mình.
Kim loại là gì?
Kim loại (tiếng Hy Lạp là metallon) là nguyên tố có thể tạo ra các ion dương (cation) và có các liên kết kim loại, và đôi khi người ta cho rằng nó tương tự như là cation trong đám mây các điện tử.
Nguyên tử là gì?
Nguyên tử là hạt nhỏ nhất của nguyên tố hóa học không thể chia nhỏ hơn được nữa về mặt hóa học.
Phi kim là gì?
Phi kim là những nguyên tố hóa học dễ nhận electron; ngoại trừ hiđrô, phi kim nằm bên phải bảng tuần hoàn.
Những sự thật thú vị về hoá học có thể bạn chưa biết
Sự thật thú vị về Hidro
Hydro là nguyên tố đầu tiên trong bảng tuần hoàn. Nó là nguyên tử đơn giản nhất có thể bao gồm một proton trong hạt nhân được quay quanh bởi một electron duy nhất. Hydro là nguyên tố nhẹ nhất trong số các nguyên tố và là nguyên tố phong phú nhất trong vũ trụ.
Sự thật thú vị về heli
Heli là một mặt hàng công nghiệp có nhiều công dụng quan trọng hơn bong bóng tiệc tùng và khiến giọng nói của bạn trở nên vui nhộn. Việc sử dụng nó là rất cần thiết trong y học, khí đốt cho máy bay, tên lửa điều áp và các tàu vũ trụ khác, nghiên cứu đông lạnh, laser, túi khí xe cộ, và làm chất làm mát cho lò phản ứng hạt nhân và nam châm siêu dẫn trong máy quét MRI. Các đặc tính của heli khiến nó trở nên không thể thiếu và trong nhiều trường hợp không có chất nào thay thế được heli.
Sự thật thú vị về Lithium
Lithium là kim loại kiềm rất hoạt động về mặt hóa học, là kim loại mềm nhất. Lithium là một trong ba nguyên tố được tạo ra trong BigBang! Dưới đây là 20 sự thật thú vị về nguyên tố Lithium – một kim loại tuyệt vời!
Sự thật thú vị về Berili
Berili (Be) có số nguyên tử là 4 và 4 proton trong hạt nhân của nó, nhưng nó cực kỳ hiếm cả trên Trái đất và trong vũ trụ. Kim loại kiềm thổ này chỉ xảy ra tự nhiên với các nguyên tố khác trong các hợp chất.
Sự thật thú vị về Boron
Boron là nguyên tố thứ năm của bảng tuần hoàn, là một nguyên tố bán kim loại màu đen. Các hợp chất của nó đã được sử dụng hàng nghìn năm, nhưng bản thân nguyên tố này vẫn chưa bị cô lập cho đến đầu thế kỉ XIX.
So sánh các chất hoá học phổ biến.
NaBrO và NaIO3
Điểm khác nhau về tính chất vật lý, hoá học giữa chất Natri hypobromua và chất Natri iodat
NaIO và Na2[Mg(OH)4]
Điểm khác nhau về tính chất vật lý, hoá học giữa chất Natri Hypoiodit và chất Tetraaquamagnesium(II) sodium
Pb2P2O6 và Na4P2O6
Điểm khác nhau về tính chất vật lý, hoá học giữa chất Chì hypophosphat và chất Natri hypophosphat
Pb(CH3COO)2 và NO2NH2
Điểm khác nhau về tính chất vật lý, hoá học giữa chất Chì axetat và chất Nitroamin