Oxit axit | Khái niệm hoá học
Oxit axit, hoặc anhydrid axit, là các oxit phản ứng với nước tạo thành axit, hoặc với một bazơ để tạo thành muối. Chúng là các oxit của phi kim hoặc kim loại ở trạng thái oxy hóa cao. Chúng có thể được hiểu một cách có hệ thống bằng cách lấy một oxoacid và loại bỏ nước khỏi nó, cho đến khi chỉ còn lại một oxit. Ôxít thu được thuộc nhóm chất này.
Giới thiệu
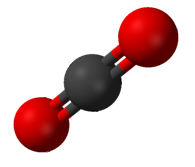
Cấu tạo một phân tử khí Cacbonic (CO2)
1. Định nghĩa
Oxit axit, hoặc anhydrid axit, là các oxit phản ứng với nước tạo thành axit, hoặc với một bazơ để tạo thành muối. Chúng là các oxit của phi kim hoặc kim loại ở trạng thái oxy hóa cao. Chúng có thể được hiểu một cách có hệ thống bằng cách lấy một oxoacid và loại bỏ nước khỏi nó, cho đến khi chỉ còn lại một oxit. Ôxít thu được thuộc nhóm chất này. Ví dụ, anhydrit axit sunfurơ (SO2), anhydrid axit sunfuric (SO3) và anhydrid axit carbonic (CO2) là các oxit axit. Một anhydride vô cơ (một thuật ngữ hơi cổ xưa) là một anhydrid axit không có thành phần hữu cơ.
Các oxit có tính axit không phải là axit Lowry-Brønsted vì chúng không cho đi proton; tuy nhiên, chúng là axit Arrhenius vì chúng làm tăng nồng độ ion hydro của nước. Ví dụ, carbon dioxide làm tăng nồng độ ion hydro của nước mưa (pH = 5,6) lên 25 lần so với nước tinh khiết (pH = 7). Chúng cũng là axit Lewis, vì chúng chấp nhận các cặp electron từ một số bazơ Lewis, đáng chú ý nhất là các anhydrua bazơ.
Các oxit của nguyên tố chu kỳ 3 thể hiện tính tuần hoàn liên quan đến tính axit. Khi một người di chuyển trong suốt thời gian, các oxit trở nên có tính axit hơn. Oxit natri và magiê có tính kiềm. Các oxit nhôm là chất lưỡng tính (phản ứng cả dưới dạng bazơ hoặc axit). Các oxit silic, phốt pho, lưu huỳnh và clo có tính axit. Một số oxit phi kim loại, chẳng hạn như oxit nitơ (N2O) và carbon monoxide (CO), không hiển thị bất kỳ đặc tính axit / bazơ nào.
Các oxit axit cũng có thể phản ứng với các oxit bazơ để tạo ra muối của oxoanions:
2 MgO + SiO2 → Mg2SiO4
Các oxit axit có ý nghĩa lớn đối với môi trường. Lưu huỳnh oxit và nitơ oxit được coi là chất gây ô nhiễm không khí khi chúng phản ứng với hơi nước trong khí quyển để tạo ra mưa axit.
2. Tính chất hóa học
– Tính tan
Đa số các oxit axit khi hoà tan vào nước sẽ tạo ra dung dịch axit trừ SiO2:
(Phản ứng thuận nghịch)
– Tác dụng với oxit bazơ tan
– Tác dụng với bazơ tan
Tuỳ vào tỉ lệ mol giữa oxit axit và bazơ phản ứng sẽ cho ra nước + muối trung hoà, muối axit hay hỗn hợp muối
Thí dụ:
Tổng số đánh giá:
Xếp hạng: / 5 sao
Chia sẻ
Các khái niệm hoá học liên quan
Chuỗi phản ứng hóa học
Sơ đồ chuỗi phản ứng là chuỗi các phản ứng thể hiện sự chuyển hóa giữa các đơn chất và hợp chất. Chuỗi phản ứng là một công cụ hữu ích trong dạy học, chúng giúp người dạy lẫn người học có thể hệ thống hóa kiến thức, tăng cường khả năng ghi nhớ
Liên kết ba
Liên kết ba là liên kết được hình thành do 3 cặp electron liên kết. Trong liên kết ba có 1 liên kết σ và 2 liên kết π.
Đồng đen
Một số tài liệu khoa học chia đồng thành 4 loại, gồm đồng đỏ, đồng thau, hợp kim đồng gạch niken và đồng đen. Đồng đen là hợp kim của đồng và thiếc, đôi lúc có cả kẽm, dùng để đúc tượng. Nhiều kim loại gặp lạnh thì co lại, nhưng đồng đen gặp lạnh lại nở ra. Đồng đen có khả năng chống mài mòn cao nên còn dùng để chế tạo các ổ bi.
Liên kết đôi
Liên kết đôi là liên kết hóa học giữa hai nguyên tử, được tạo bởi một liên kết sigma (hay liên kết đơn) và một liên kết pi. Liên kết đôi bền và khó phá vỡ hoàn toàn hơn liên kết đơn, nhưng lại dễ tham gia phản ứng hóa học hơn do chứa liên kết pi dễ bị phá vỡ hơn liên kết sigma.
Chất
Chất có khắp nơi, ở đâu có vật thể là ở đó có chất. Mỗi chất (tinh khiết) có những tính chất vật lí và hóa học nhất định.
Một số định nghĩa cơ bản trong hoá học.
Mol là gì?
Trong hóa học, khái niệm mol được dùng để đo lượng chất có chứa 6,022.10²³ số hạt đơn vị nguyên tử hoặc phân tử chất đó. Số 6,02214129×10²³ – được gọi là hằng số Avogadro.
Độ âm điện là gì?
Độ âm điện là đại lượng đặc trưng định lượng cho khả năng của một nguyên tử trong phân tử hút electron (liên kết) về phía mình.
Kim loại là gì?
Kim loại (tiếng Hy Lạp là metallon) là nguyên tố có thể tạo ra các ion dương (cation) và có các liên kết kim loại, và đôi khi người ta cho rằng nó tương tự như là cation trong đám mây các điện tử.
Nguyên tử là gì?
Nguyên tử là hạt nhỏ nhất của nguyên tố hóa học không thể chia nhỏ hơn được nữa về mặt hóa học.
Phi kim là gì?
Phi kim là những nguyên tố hóa học dễ nhận electron; ngoại trừ hiđrô, phi kim nằm bên phải bảng tuần hoàn.
Những sự thật thú vị về hoá học có thể bạn chưa biết
Sự thật thú vị về Hidro
Hydro là nguyên tố đầu tiên trong bảng tuần hoàn. Nó là nguyên tử đơn giản nhất có thể bao gồm một proton trong hạt nhân được quay quanh bởi một electron duy nhất. Hydro là nguyên tố nhẹ nhất trong số các nguyên tố và là nguyên tố phong phú nhất trong vũ trụ.
Sự thật thú vị về heli
Heli là một mặt hàng công nghiệp có nhiều công dụng quan trọng hơn bong bóng tiệc tùng và khiến giọng nói của bạn trở nên vui nhộn. Việc sử dụng nó là rất cần thiết trong y học, khí đốt cho máy bay, tên lửa điều áp và các tàu vũ trụ khác, nghiên cứu đông lạnh, laser, túi khí xe cộ, và làm chất làm mát cho lò phản ứng hạt nhân và nam châm siêu dẫn trong máy quét MRI. Các đặc tính của heli khiến nó trở nên không thể thiếu và trong nhiều trường hợp không có chất nào thay thế được heli.
Sự thật thú vị về Lithium
Lithium là kim loại kiềm rất hoạt động về mặt hóa học, là kim loại mềm nhất. Lithium là một trong ba nguyên tố được tạo ra trong BigBang! Dưới đây là 20 sự thật thú vị về nguyên tố Lithium – một kim loại tuyệt vời!
Sự thật thú vị về Berili
Berili (Be) có số nguyên tử là 4 và 4 proton trong hạt nhân của nó, nhưng nó cực kỳ hiếm cả trên Trái đất và trong vũ trụ. Kim loại kiềm thổ này chỉ xảy ra tự nhiên với các nguyên tố khác trong các hợp chất.
Sự thật thú vị về Boron
Boron là nguyên tố thứ năm của bảng tuần hoàn, là một nguyên tố bán kim loại màu đen. Các hợp chất của nó đã được sử dụng hàng nghìn năm, nhưng bản thân nguyên tố này vẫn chưa bị cô lập cho đến đầu thế kỉ XIX.
So sánh các chất hoá học phổ biến.
ClF5 và ClO3F
Điểm khác nhau về tính chất vật lý, hoá học giữa chất Clo pentaflorua và chất Percloryl florua
Cl2O3 và Cl2O6
Điểm khác nhau về tính chất vật lý, hoá học giữa chất Diclo trioxit và chất Diclorine hexoxit
Cl2O7 và CoAl2O4
Điểm khác nhau về tính chất vật lý, hoá học giữa chất Diclo heptoxit và chất Coban(II) aluminat
CoAs và CoB
Điểm khác nhau về tính chất vật lý, hoá học giữa chất Monocoban monoarsenua và chất Coban monoborua
